Corp. Substanță. Amestec
1. Chimia - știință experimentală
Chimia s-a constituit ca ramură a științei la sfârșitul secolului al XVIII-lea și începutul secolului al XIX-lea, pe de o parte ca urmare a volumului mare de descoperiri din domeniul substanțelor naturale și al substanțelor sintetizate în laborator, iar, pe de altă parte, ca urmare a enunțării principiilor și legilor fundamentale din domeniul transformărilor de substanțe.
Ca urmare a volumului extrem de mare de cunoștințe acumulate, în secolul al XIX-lea se conturează deja două ramuri ale chimiei: chimia anorganică, chimia substanțelor existente preponderent în regnul mineral, și chimia organică, chimia substanțelor sintetizate, cu precădere, în organismele vii.
Prin chimie, omul și-a făcut viața mai plăcută, și-a înțeles propria viață, s-a înarmat față de vitregiile existente și viitoare.
Chimia modernă a contribuit substanțial la creșterea calității vieții, prin elaborarea în condiții avantajoase a unei game largi de materiale: materiale plastice, săpunuri, detergenți, medicamente, alimente prelucrate, îngrășăminte, combustibili nucleari, etc.
În prezent, chimia este o știință complexă extinsă spre multe alte discipline.
Saltul tehnologic și cercetările în domeniu au determinat apariția unor ramuri noi: biochimia, chimia-fizică, chimia farmaceutică, chimia medicală, geochimia, agrochimia, chimia nucleară, radiochimia.
Chimia este una din ramurile științelor naturii – alături de matematică, fizică și biologie.
Mai mult ca oricare știință a naturii, chimia este legată de tot ceea ce ne înconjoară.
Pentru viitor, chimia, împreună cu celelalte ramuri ale științei, este chemată să contribuie la găsirea unor soluții optime pentru marile provocări ale lumii moderne:
a) resurse de hrană pentru populația Terrei;
b) resurse de apă potabilă și tehnici viabile de desalinizare a apei de mare;
c) combustibili mai puțin poluanți sau total nepoluanți;
d) îngrășăminte chimice, pesticide, fungicide, mai puțin agresive cu organismul uman și cu mediul înconjurător;
e) tehnici optime de reciclare a deșeurilor;
f) diminuarea efectului de seră și a încălzirii globale;
g) medicamente și produse farmaceutice revoluționare;
h) materiale pentru construirea de spații locuibile pe alte planete, în subteran sau în mediul acvatic.
2. Momente din evoluția chimiei ca știință
a) Descoperirea focului
Deși nu se cunoaște nici locul, nici cine a descoperit focul, arderea lemnelor a fost utilizată încă din cele mai vechi timpuri pentru prepararea hranei și prelucrarea metalelor.
b) Descoperirea primelor elemente chimice
Inițial, au fost descoperite metale care se găsesc în stare liberă în natură: aurul, argintul, mercurul.
Au urmat apoi pucioasa și cărbunele.
c) Descoperirea experimentului chimic de laborator și folosirea balanței au permis descoperirea legilor de bază ale chimiei.
d) Descoperirea teoriei atomo-moleculare
Noțiunea de atom, ca fiind cea mai mică particulă, a stat la baza descoperirii structurii substanțelor.
e) Marile descoperiri de la sfârșitul secolului al XIX-lea:
⮚ electronul, particulă elementară negativă, componentă a atomului ;
⮚ radioactivitatea, proprietatea unor elemente de a emite spontan și continuu radiații ;
⮚ teoria cuantelor: lumina este emisă în mod discontinuu sub formă de ,,cuantă” de lumină
f) Marile descoperiri ale secolului al XX-lea:
⮚ procesul de fotosinteză reușește să obțină din câteva elemente o gamă vastă de substanțe: glucoză, zahăr, amidon, celuloză, grăsimi, uleiuri, esențe parfumate, coloranți, vitamine, etc.
⮚ hârtia se fabrică din lemn, paie sau stuf.⮚ procesele fermentative au fost observate încă din cele mai vechi timpuri și utilizate în gospodărie
⮚ vitaminele se găsesc în cantități extrem de mici în alimente, dar care sunt strict necesare organismului uman. Ele sunt sintetizate de industria farmaceutică.
⮚ lumea maselor plastice a apărut, s-a dezvoltat și are un viitor pe care numai chimiștii pot să-l întrezărească. Ele sunt folosite din ce în ce mai mult în locul materialelor naturale.
3. Materie. Corp. Substanță. Material
Materia reprezintă realitatea care există independent de noi și constituie izvorul tuturor transformărilor din natură.
Proprietăți ale materiei:
⮚ ocupă un spațiu ;
⮚ prezintă o masă proprie ;
⮚ se găsește în continuă mișcare și transformare ;
⮚ apare sub diferite forme ;
⮚ nu dispare și nu se creează.
Porțiuni limitate din materie cu formă și volum bine determinat poartă numele de corpuri.
Exemple de corpuri:
⮚ apa dintr-un pahar
⮚ o bancă
⮚ o casă
⮚ o piatră
⮚ aerul dintr-o minge
Formele omogene de materie cu o compoziție constantă se numesc substanțe.
Exemple de substanțe:
⮚ oxigen
⮚ apă
⮚ aur
⮚ dioxid de carbon
⮚ azot
Formele eterogene de materie cu o compoziție variabilă se numesc materiale.
Exemple de materiale:
⮚ sticlă
⮚ lemn
⮚ beton
⮚ ciment
4. Ustensile de laborator
Chimia este o știință experimentală.
Pentru a putea efectua experimente chimice avem nevoie de un laborator de chimie, de ustensile și aparatură de laborator.
Ustensilele și aparatura de laborator se clasifică în:
a) confecționate din sticlă : eprubete, pahar Berzelius, pahar Erlenmeyer, sticla de ceas, cilindru gradat, cristalizor, bagheta de sticlă
b) confecționate din porțelan : creuzet, mojar cu pistil, capsulă
c) confecționate din lemn : clește, stativ pentru eprubete
d) confecționate din fier : balanță, trepied, sită de azbest, becul de gaz.
5. Proprietăți fizice și chimice ale substanțelor
Numărul substanțelor este foarte mare.
Acestea se deosebesc între ele prin însușirile pe care le au: gust, culoare, stare de agregare, miros, densitate, însușirea de a arde, etc.
Însușirile caracteristice, cu ajutorul cărora se recunoaște o substanță, se numesc proprietăți.
Proprietățile pot fi:
a) proprietăți fizice: miros, culoare, formă, stare de agregare, densitate, punct de fierbere, punct de topire, ș.a.
b) proprietăți chimice: proprietatea de a arde, proprietatea de a rugini, proprietatea de a fermenta, ș.a.
Proprietățile care se referă la transformări care nu pot să nu modifice compoziția substanței se numesc proprietăți fizice.
Proprietățile care se referă la transformări care pot să modifice compoziția substanței se numesc proprietăți chimice.
6. Fenomene fizice și chimice
Transformările pe care le suferă o substanță se numesc fenomene.
Fenomenele care modifică compoziția substanțelor, transformându-le în substanțe cu proprietăți noi, se numesc fenomene chimice.
Exemple: râncezirea grăsimilor, fermentarea laptelui, coclirea vaselor de aramă, fotosinteza, etc.
Fenomenele care nu modifică compoziția substanțelor se numesc fenomene fizice.
Exemple: modificarea stării de agregare, dilatarea substanțelor, spargerea unui geam, ruperea unei hârtii, dizolvarea, etc.
7. Substanțe și amestecuri
În natură, materia se găsește în diferite forme.
Prin luarea împreună a două sau mai multe substanțe între care nu au loc fenomene chimice se obțin amestecuri de substanțe.
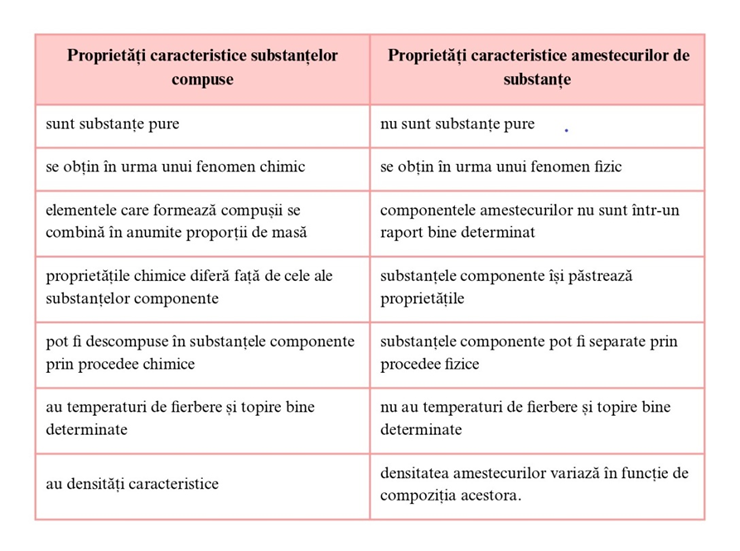
Majoritatea substanțelor se găsesc în natură sub formă de amestecuri.
Exemple: apa potabilă, apa minerală, aerul, rocile, minereurile, apa mării, petrolul, cărbunii, sarea gemă, aliajele, etc.
Amestecurile se pot clasifica în :
a) amestecuri omogene: au în toată masa lor aceeași compoziție și aceleași proprietăți
b) amestecuri eterogene: au compoziție diferită în masa lor și proprietăți diferite.
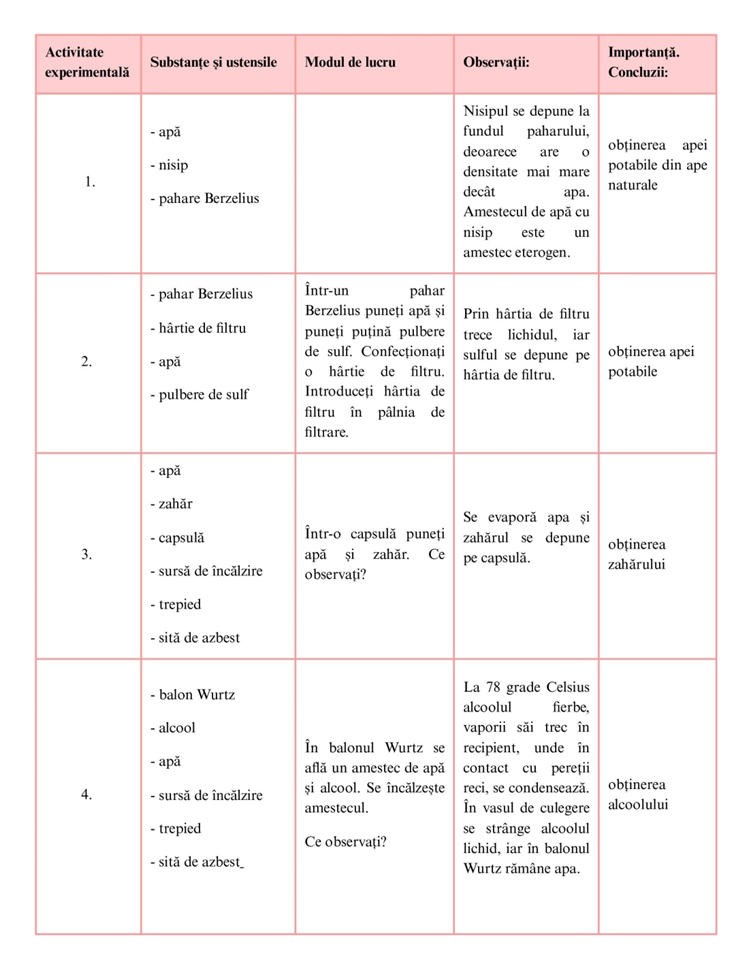
8. Metode de separare a substanțelor din amestecuri
Reţineţi:
a) Operația de separare a unei substanțe solide, cu densitate mare și insolubilă în lichidul în care se găsește se numește decantare.
b) Operația de separare, printr-un filtru, a unei substanțe solide, insolubile, dar cu densitate apropiată de cea a lichidului în care se găsește, se numește filtrare.
c) Operația de trecere a unei substanțe din soluție în stare solidă, la cald, se numește cristalizare.
d) Operația de purificare a substanțelor, prin separarea componentelor dintr-un amestec de lichide, prin fierbere urmată de condensare se numește distilare.